گلبول های سفید یا لکوسیت ها اولین و دومین خط دفاعی بدن در برابر ارگانیسم ها و ذرات خارجی هستند. با این حال، داروهای کمی تولید و حرکت این سلول ها را برای اهداف مفید بالینی هدف قرار می دهند. مطالعه جدیدی که در مجله منتشر شده است مصونیت چشم انداز مولکول سیگنال را برای شناسایی اهداف بالقوه قابل دارو برای مهاجرت لکوسیت ها به جریان خون بررسی می کند.
مطالعه: مهار مولکول کوچک CBP/p300 هیستون استیل ترانسفراز، لکوسیت ها را از مغز استخوان از طریق پاسخ استرس غدد درون ریز بسیج می کند.. اعتبار تصویر: Rost9 / Shutterstock
لکوسیت ها، از جمله نوتروفیل ها، مونوسیت ها و لنفوسیت های B، در مغز استخوان از سلول های پیش ساز خون ساز و در چند اندام تخصصی دیگر تشکیل می شوند. آنها در مغز استخوان نگه داشته می شوند تا زمانی که به گردش خون رها شوند.
دو محفظه لکوسیتی در خون و بافتهای محیطی وجود دارد که با حالتهای مختلف بدن تغییراتی را در اندازه نشان میدهند. به عنوان مثال، هنگامی که بدن آسیب می بیند، تحت فشار قرار می گیرد یا آلوده می شود، تعداد لکوسیت ها در بافت آسیب دیده تغییر می کند و پس از مهار تهدید به حالت عادی باز می گردد.
مراحل تنظیمی متعددی در تجزیه لکوسیت ها و همچنین حرکت به مکان های مختلف که در آن مورد نیاز است، شرکت می کنند. اینها در سیستم عصبی مرکزی (CNS) در پاسخ به سیگنالهای محیطی منشأ میگیرند و توسط مدارهای عصبی تنظیم میشوند که هم سیستم عصبی سمپاتیک و هم محور هیپوتالاموس-هیپوفیز-آدرنال (HPA) در آن مشارکت دارند.
این سیگنالها برای افزایش خونسازی مغز استخوان، جذب لکوسیتها در خون و سایر بافتهای مورد نیاز، و اطمینان از بازگشت آنها به سطوح طبیعی پس از رفع چالش کار میکنند.
در برخی شرایط بیماری، این کنترل هموستاتیک از دست میرود، بنابراین منجر به شمارش غیرطبیعی میشود، مانند نارسایی مغز استخوان از یک سو یا لوسمی حاد از سوی دیگر. با این حال، هنوز تعداد کمی از داروها می توانند با اصلاح سرعت تولید، تجزیه، یا مهاجرت لکوسیت ها، چه در سرطان خون، التهاب مزمن، یا حالت های بیش التهابی حاد، به اصلاح چنین بی نظمی کمک کنند.
از جمله داروهای موجود میتوان به خانواده فاکتور محرک کلنی گرانولوسیت (G-CSF)، آنتاگونیستهای گیرنده کموکاین 4 با موتیف CXC (CXCR4) مانند plerixafor/AMD3100 یا مهارکنندههای آنتیژن بسیار دیررس اینتگرین 4 (VLA4) اشاره کرد. به عنوان مثال، G-CSF برای اصلاح نوتروپنی در بیماران تحت شیمی درمانی استفاده می شود، اما در بیماران مبتلا به بیماری های تب دار حاد شامل تعداد کم نوتروفیل ها کمتر مفید است. علاوه بر این، G-CSF می تواند عوارض جانبی در برخی از بیماران ایجاد کند.
نیاز به دانستن بیشتر در مورد این رشته از فارماکولوژی انگیزه مطالعه حاضر شد. این مولکول بر روی یک مولکول کوچک به نام پروتئین P300 مرتبط با E1A (EP300 یا p300) تمرکز می کند که به تازگی در مرحله لوسمی وضعیتی به نام نوتروپنی مادرزادی شدید (SCN) به دست آمده است.
از دست دادن عملکرد این ژن منجر به کاهش تولید سلولهای خونی در صورت حذف قبل از تولد شده، اما تعداد لکوسیتهای لوسمی بالا یا لوکوسیت در سنین بالاتر افزایش مییابد. این دارای یک پروتئین پیوند دهنده ارتولوگ، حلقوی-آدنوزین-مونوفسفات-پاسخ به عنصر (CREBBP، که به عنوان “CBP” نیز شناخته می شود، با 90% همسانی توالی است. یکی از 8 حوزه در این ژن مسئول هیستون استیل ترانسفراز (HAT) است. فعالیت و حاوی یک جهش در SCN است که باعث تبدیل لوسمی می شود.
در این مورد، این دامنه ممکن است قابل تولید دارو باشد.لکوسیتوز در صورت تقاضابا تغییر اندازه بخش های مختلف لکوسیت.
مطالعه چه چیزی را نشان داد؟
دانشمندان دریافتند که مهار دامنه CBP/p300 با فعالیت HAT توسط بازدارنده مولکولی کوچک A485 منجر به مهار رقابتی برگشت پذیر فعالیت آنزیم HAT، به ویژه برای CBP و p300 در مقایسه با سایر HAT ها شد. همانطور که انتظار می رفت، این منجر به افزایش سریع سطح استیل CoA در ماکروفاژهای مغز استخوان در مدل های موش شد. نتیجه لکوسیتوز سریع بود.
مشخص شد که این یک عمل وابسته به دوز است و با تجویز مکرر از بین نمی رود. هنگامی که نوع دیگری از مهارکننده CBP/p300 HAT (C646) استفاده شد، همان اثر مشاهده شد که مکانیسم اثر را تأیید میکند. برعکس، مهارکنندههای اتصال DNA توسط پروتئین یا HAT دیگری که در پستانداران یافت میشود نتوانستند باعث لکوسیتوز شوند.
سطح A485 در خون با تزریق به موش ها به سرعت افزایش می یابد و در مغز استخوان، بافت چربی، کبد، طحال و کلیه تجمع می یابد، اما نه در مغز. تعداد لکوسیت ها به موازات افزایش یافت، از جمله نوتروفیل ها، لنفوسیت ها و مونوسیت ها. یک هفته بعد، هیچ شواهدی از تجویز دارو قابل مشاهده نبود که نشان دهنده یک اثر گذرا باشد.
افزایش تعداد لکوسیت ها با آنچه توسط G-CSF به دست آمد قابل مقایسه بود، هرچند برای نوتروفیل ها تا حدودی سریعتر بود. هنگامی که هر دو داده شدند، تعداد نوتروفیل ها به طور قابل توجهی بالاتر بود. با این حال، پس از 24 ساعت، هر سه نوع سلول خونی با G-CSF در مقابل A485 افزایش یافت.
این نشان دهنده عملکرد کوتاهتر و متفاوت A485 در مقایسه با G-CSF است.
برای گسترش مشاهدات به افراد انسانی، محققان به دادههای گروهی از بیماران مبتلا به یک بیماری نادر به نام سندرم روبینشتاین طیبی (RSTS) نگاه کردند. CREBBP و EP300 جهش رخ می دهد. حدود دو سوم تعداد لکوسیتهای بالایی داشتند و 70 درصد جهشهایی را در دامنه HAT نشان میدادند. همانطور که انتظار می رفت، احتمال بروز لکوسیتوز در این گروه بیشتر از گروه دیگر بود که در آن HAT در امان بود.
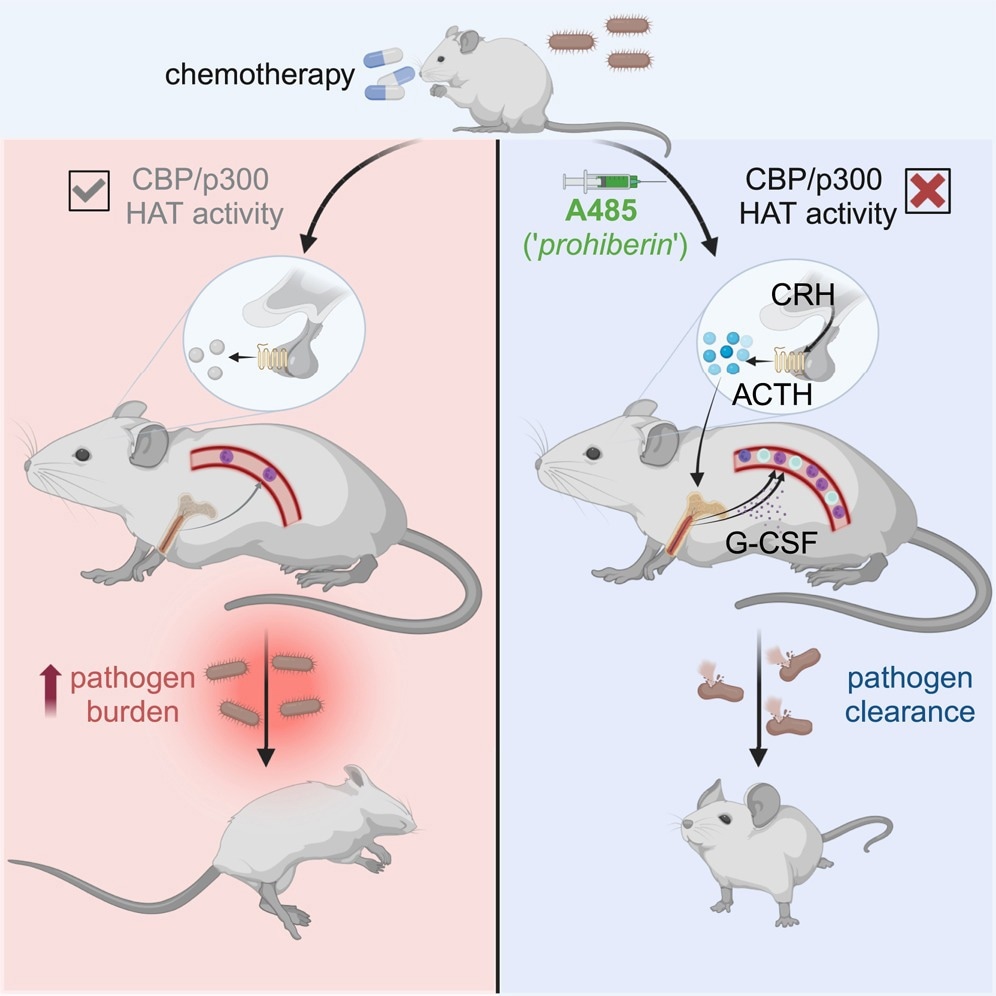
آیا این مشاهده کاربرد بالینی دارد؟ برای پی بردن به این موضوع، آنها تأثیر A485 را در گروهی از موشهای مبتلا به سندرم میلودیسپلاستیک (MDS) آزمایش کردند و دریافتند که این مولکول کوچک تعداد لکوسیتها را نرمال نگه میدارد. ثانیاً، آنها با یک دوره شیمی درمانی در یک مدل موش، نوتروپنی شدید را القا کردند که نشان داد A485 منجر به بازیابی حاد تعداد لکوسیت ها شد.
سپس ارگانیسم را معرفی کردند لیستریا مونوسیتوژنز در یک دوز تحریک کننده سپسیس در موش های مبتلا به پان سیتوپنی ناشی از شیمی درمانی. نوتروفیل ها برای دفاع ایمنی در برابر این میکروب حیاتی هستند. پس از ایجاد عفونت، A485 را در مقابل وسیله نقلیه در کنترل ها تزریق کردند.
در حالی که افراد تحت درمان با وسیله نقلیه بیمار شدند و به دلیل سپسیس جان خود را از دست دادند، A485 در یک دوز واحد منجر به بهبود بقا شد و باکتری های کمتری از حیوانات تحت درمان بازیابی شد. A485 لکوسیت ها را از مغز استخوان بسیج می کند، که مکانیسم لکوسیتوز است. در مقابل، خونسازی اضطراری در مغز استخوان وجود نداشت.
زیرمجموعههای مختلف لکوسیتها به مسیرهای متمایز ایجاد شده توسط A485 پاسخ دادند. اینها هم مسیرهای وابسته به G-CSF و هم مسیرهای مستقل نوتروفیلی را شامل می شوند، اما مسیرهای دیگری برای لنفوسیتوز را شامل می شوند.
علاوه بر این، A485 از مسیرهای عصبی-هومورال، به ویژه محور HPA، برای القای لکوسیتوز استفاده می کند، همانطور که با افزایش سطوح گلوکوکورتیکوئیدها در خون پس از تجویز A485 مشاهده می شود. پاسخ لکوسیتوز ناشی از فعالسازی HPA به گلوکوکورتیکوئیدها متکی نیست، اما در پاسخ به سیگنالهای تنظیمشده با CRHR1، از جمله هورمون آدرنوکورتیکوتروپیک (ACTH)، که با از دست دادن سیگنالهای بازخورد HPA رخ میدهد، رخ میدهد.
در حالی که نوتروفیل ها با تجویز ACTH افزایش می یابد، تعداد لنفوسیت ها تنها با مسدود کردن گلوکوکورتیکوئید افزایش می یابد، که نشان می دهد هر دو به طور متفاوتی تنظیم می شوند.
چه پیامدهایی دارد؟
“مهار رقابتی، برگشتپذیر و با واسطه مولکولهای کوچک دامنه HAT CBP/p300 باعث حرکت حاد و گذرا لکوسیت از مغز استخوان میشود.تحقیقات بیشتری برای شناسایی زمینههای بالینی ایدهآل برای این دارو مورد نیاز است. اگر فقط به افزایش سریع نوتروفیلها نیاز باشد، ممکن است A485 بهتر باشد، در حالی که بازیابی طولانیمدت تولید سلولهای خونی در مغز استخوان ممکن است نیاز به G- داشته باشد. CSF.
زمان تجویز برای نتایج خوب نیز باید تعریف شود زیرا بیماران مبتلا به سپسیس نوتروپنیک در مقاطع زمانی و مراحل مختلف حضور دارند. علاوه بر این، ارزش چنین داروهایی در سپسیس باکتریایی یا ویروسی، به جای لیستریال، ناشناخته باقی مانده است.
با این حال، همانطور که توسط محققان قبلی گزارش شده است، دارای اثرات ضد توموری است که می تواند آن را در درمان کمکی برای بیماران سرطانی ارزشمند کند. مطالعه حاضر همچنین نقش ACTH، به جای محصولات پایین دستی آن، گلوکوکورتیکوئیدها، بر هموستاز لکوسیت ها و فعالیت G-CSF را روشن می کند.
